Ion là gì và phân loại cơ bản
Khái niệm ion trong hóa học
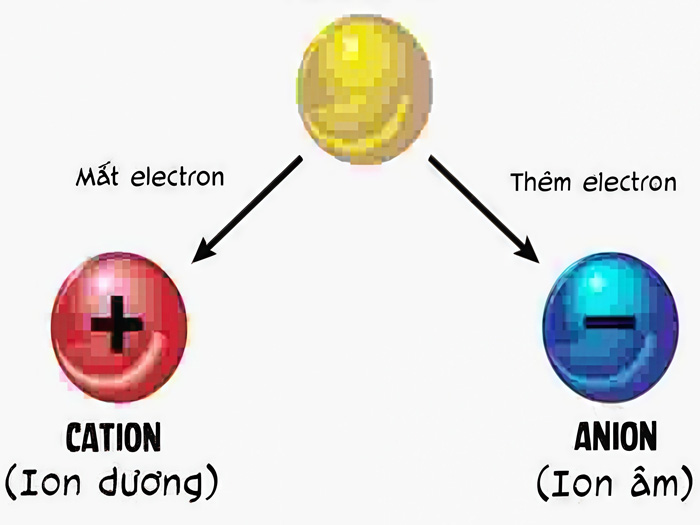
Trong hóa học, ion là nguyên tử hoặc nhóm nguyên tử mang điện tích do mất hoặc nhận electron. Đây là nền tảng quan trọng để hiểu cách xác định điện tích ion một cách chính xác.
- Khi nguyên tử trung hòa (số proton = số electron)
- Nếu mất electron → số proton > số electron → mang điện dương
- Nếu nhận electron → số electron > số proton → mang điện âm
Điểm cốt lõi:
→ Điện tích ion phụ thuộc trực tiếp vào sự chênh lệch giữa proton và electron
Ví dụ:
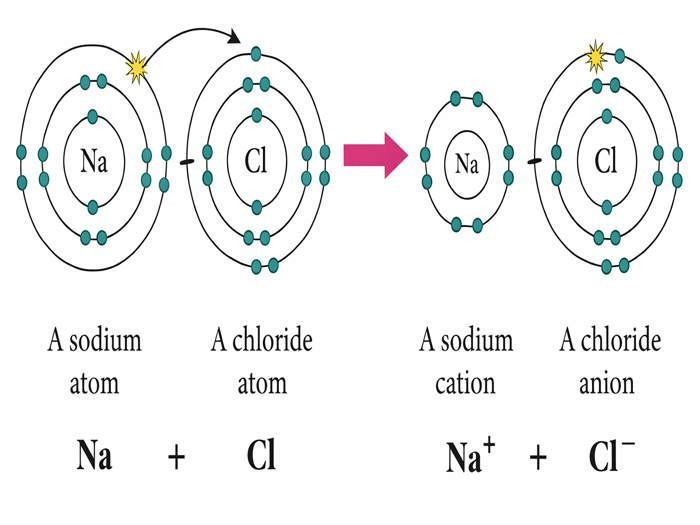
- Na (11e) mất 1e → Na⁺
- Cl (17e) nhận 1e → Cl⁻
Đây là bước đầu giúp người học hiểu bản chất trước khi áp dụng quy tắc nhanh.
Phân biệt ion dương và ion âm
Dựa vào cách nguyên tử thay đổi electron, ion được chia thành 2 loại chính:
Ion dương (cation):
- Hình thành khi mất electron
- Thường là kim loại
- Điện tích mang dấu “ ”
Ion âm (anion):
- Hình thành khi nhận electron
- Thường là phi kim
- Điện tích mang dấu “−”
Quy luật dễ nhớ:
- Kim loại → cho electron → dương
- Phi kim → nhận electron → âm
Đây là quy tắc cực kỳ quan trọng giúp rút ngắn thời gian xác định điện tích trong bài tập trắc nghiệm.
Vai trò electron trong hình thành ion
Electron lớp ngoài cùng (electron hóa trị) quyết định toàn bộ việc hình thành ion.
Nguyên tắc cơ bản:
- Nguyên tử luôn có xu hướng đạt cấu hình bền (giống khí hiếm)
- Để đạt trạng thái này, nguyên tử sẽ:
- Mất electron (nếu có ít electron ngoài cùng)
- Nhận electron (nếu gần đủ 8e)
Ví dụ:
- Na có 1 electron lớp ngoài → dễ mất → Na⁺
- O có 6 electron lớp ngoài → cần thêm 2e → O²⁻
Kết luận nhanh: → Số electron mất/nhận = độ lớn điện tích ion
Quy tắc xác định điện tích ion nhanh
Dựa vào nhóm nguyên tố trong bảng tuần hoàn
Đây là cách nhanh nhất, thường dùng trong thi cử.
Các nhóm chính có quy luật rõ ràng:
- Nhóm IA (1): 1
- Nhóm IIA (2): 2
- Nhóm IIIA (13): 3
- Nhóm VA (15): −3
- Nhóm VIA (16): −2
- Nhóm VIIA (17): −1
Ví dụ:
- K (nhóm IA) → K⁺
- Ca (nhóm IIA) → Ca²⁺
- Cl (nhóm VIIA) → Cl⁻
Mẹo nhớ nhanh:
- Nhóm bên trái → dương
- Nhóm bên phải → âm
Quy tắc mất và nhận electron
Nếu không nhớ nhóm, bạn vẫn có thể xác định điện tích bằng logic electron.
Các bước:
- Xác định số electron lớp ngoài cùng
- So với cấu hình bền (8e)
- Tính số electron cần mất/nhận
Nguyên tắc:
- Mất n electron → ion n
- Nhận n electron → ion −n
Ví dụ:
- Mg có 2e ngoài → mất 2e → Mg²⁺
- N có 5e ngoài → nhận 3e → N³⁻
Cách này đặc biệt hữu ích khi gặp nguyên tố ít quen thuộc.
Mối liên hệ giữa điện tích và cấu hình electron
Hiểu sâu hơn, điện tích ion luôn liên quan đến việc đạt cấu hình khí hiếm gần nhất.
Ví dụ:
- Na (Z=11): 2-8-1 → mất 1e → 2-8 (giống Ne) → Na⁺
- O (Z=8): 2-6 → nhận 2e → 2-8 (giống Ne) → O²⁻
Điều này cho thấy: → Ion không hình thành ngẫu nhiên, mà tuân theo quy luật ổn định năng lượng
Cách xác định điện tích ion kim loại
Kim loại nhóm IA, IIA dễ nhớ
Đối với kim loại nhóm chính, việc xác định điện tích ion gần như có thể làm ngay lập tức mà không cần tính toán.
Quy tắc cốt lõi:
- Nhóm IA (kim loại kiềm): luôn tạo ion 1
- Nhóm IIA (kim loại kiềm thổ): luôn tạo ion 2
Nguyên nhân:
- Các nguyên tố này có số electron lớp ngoài rất ít (1 hoặc 2)
- Dễ dàng mất electron để đạt cấu hình bền
Ví dụ:
- Na → Na⁺
- K → K⁺
- Ca → Ca²⁺
- Mg → Mg²⁺
Mẹo nhớ nhanh: → Kim loại đứng càng trái bảng tuần hoàn → càng dễ mất electron → điện tích càng đơn giản
Kim loại chuyển tiếp cần lưu ý gì
Khác với nhóm IA, IIA, kim loại chuyển tiếp (d-block) có thể có nhiều điện tích khác nhau, khiến việc xác định phức tạp hơn.
Ví dụ điển hình:
- Fe: 2 hoặc 3
- Cu: 1 hoặc 2
- Zn: 2 (ổn định nhất)
Nguyên nhân:
- Electron không chỉ nằm ở lớp ngoài cùng mà còn liên quan đến phân lớp d
- Sự phân bố electron linh hoạt → tạo nhiều trạng thái oxi hóa
Cách xử lý nhanh:
- Ghi nhớ các ion phổ biến nhất trong chương trình học
- Dựa vào hợp chất cụ thể để suy ra điện tích
Ví dụ:
- FeCl₂ → Fe²⁺
- FeCl₃ → Fe³⁺
Kết luận: → Với kim loại chuyển tiếp, không nên đoán mà cần dựa vào dữ kiện bài toán
Các trường hợp ngoại lệ phổ biến
Một số nguyên tố không tuân theo quy tắc “một điện tích cố định”, cần đặc biệt lưu ý:
- Al (nhôm): luôn 3
- Zn (kẽm): luôn 2
- Ag (bạc): thường 1
Ngoài ra:
- Sn, Pb có thể có 2 và 4
- Fe, Cu có nhiều mức điện tích như đã đề cập
Mẹo học hiệu quả:
- Không học lan man tất cả nguyên tố
- Chỉ tập trung vào các nguyên tố xuất hiện nhiều trong bài tập
Cách xác định điện tích ion phi kim
Quy tắc nhận electron của phi kim
Phi kim có xu hướng nhận electron để đạt cấu hình bền (8 electron lớp ngoài).
Nguyên tắc:
- Số electron cần nhận = 8 − số electron lớp ngoài
- Điện tích ion = số electron nhận (mang dấu âm)
Ví dụ:
- O (6e ngoài) → nhận 2e → O²⁻
- N (5e ngoài) → nhận 3e → N³⁻
Điểm cần nhớ: → Phi kim càng gần nhóm VIII (khí hiếm) → càng dễ nhận electron
Nhóm VIIA, VIA thường gặp
Đây là hai nhóm phi kim xuất hiện nhiều nhất trong bài tập.
Nhóm VIIA (halogen):
- Có 7e ngoài → nhận 1e → điện tích −1
- Ví dụ: Cl⁻, F⁻, Br⁻
Nhóm VIA:
- Có 6e ngoài → nhận 2e → điện tích −2
- Ví dụ: O²⁻, S²⁻
Ngoài ra:
- Nhóm VA → nhận 3e → −3 (N³⁻, P³⁻)
Mẹo nhớ nhanh:
- 8 − số nhóm A = điện tích âm
Mẹo ghi nhớ nhanh không cần học thuộc
Thay vì học thuộc từng ion, bạn có thể áp dụng quy tắc tư duy:
- Xác định nguyên tố là kim loại hay phi kim
- Nhìn vị trí trong bảng tuần hoàn
- Suy ra xu hướng mất hay nhận electron
Quy tắc vàng:
- Kim loại → điện tích dương
- Phi kim → điện tích âm
- Tổng electron hướng về cấu hình bền
Ngoài ra, có thể dùng “quy tắc bù 8”:
- Số electron cần để đủ 8 → chính là điện tích âm
Ví dụ minh họa xác định điện tích ion
Ví dụ với kim loại đơn giản
Đây là dạng cơ bản nhất, thường gặp trong các câu hỏi lý thuyết hoặc trắc nghiệm nhanh.
Ví dụ 1: Xác định điện tích ion của Na
- Na thuộc nhóm IA
- Có 1 electron lớp ngoài
→ Mất 1 electron để đạt cấu hình bền
Kết luận: Na → Na⁺
Ví dụ 2: Xác định điện tích ion của Ca
- Ca thuộc nhóm IIA
- Có 2 electron lớp ngoài
→ Mất 2 electron
Kết luận: Ca → Ca²⁺
Nhận xét: → Với kim loại nhóm A, chỉ cần nhớ nhóm là xác định được ngay điện tích
Ví dụ với phi kim phổ biến
Phi kim thường xuất hiện trong các hợp chất ion và bài tập suy luận.
Ví dụ 1: Xác định điện tích ion của Cl
- Cl thuộc nhóm VIIA
- Có 7 electron lớp ngoài
→ Nhận thêm 1 electron
Kết luận: Cl → Cl⁻
Ví dụ 2: Xác định điện tích ion của O
- O thuộc nhóm VIA
- Có 6 electron lớp ngoài
→ Nhận thêm 2 electron
Kết luận: O → O²⁻
Nhận xét: → Phi kim luôn hướng tới nhận electron để đạt đủ 8e lớp ngoài
Ví dụ bài tập tổng hợp
Dạng này yêu cầu bạn kết hợp nhiều quy tắc để suy luận chính xác.
Ví dụ: Xác định điện tích của Fe trong hợp chất FeCl₃
Phân tích:
- Cl luôn có điện tích −1
- Có 3 nguyên tử Cl → tổng điện tích = −3
- Hợp chất trung hòa điện → tổng điện tích = 0
→ Fe phải có điện tích 3
Kết luận: Fe³⁺
Ví dụ khác: Xác định điện tích của Cu trong CuO
- O có điện tích −2
- Hợp chất trung hòa
→ Cu phải là 2
Kết luận: Cu²⁺
Điểm quan trọng: → Khi làm bài tập, luôn sử dụng nguyên tắc trung hòa điện
Mẹo học nhanh và tránh nhầm lẫn
Nhận diện nhanh dạng bài
Để làm nhanh, bạn cần phân loại bài ngay từ đầu:
- Dạng 1: Hỏi trực tiếp điện tích ion → dùng bảng tuần hoàn
- Dạng 2: Cho hợp chất → suy ra điện tích
- Dạng 3: Kết hợp nhiều nguyên tố → cần lập phương trình tổng điện tích
Việc nhận diện đúng giúp tiết kiệm rất nhiều thời gian.
Lỗi sai thường gặp khi xác định ion
Một số lỗi phổ biến khiến học sinh mất điểm:
- Nhầm kim loại và phi kim
- Quên quy tắc “bù 8 electron”
- Áp dụng sai điện tích của kim loại chuyển tiếp
- Không kiểm tra tổng điện tích trong hợp chất
Ví dụ sai điển hình:
- Cho rằng Fe luôn 2 (trong khi có thể 3)
- Nhầm O là −1 (thực tế thường là −2)
Giải pháp: → Luôn kiểm tra lại logic electron và tính trung hòa
Cách luyện tập để nhớ lâu
Để thành thạo cách xác định điện tích ion, bạn nên:
- Luyện bài tập theo từng dạng riêng
- Ghi nhớ các ion phổ biến thay vì học lan man
- Tự giải thích lại quy tắc bằng lời của mình
- Làm nhiều bài trắc nghiệm để tăng tốc độ
Phương pháp hiệu quả: → Học theo “hiểu bản chất luyện phản xạ” thay vì học thuộc lòng
Bảng tổng hợp điện tích ion thường gặp
Ion kim loại phổ biến
Một số ion kim loại xuất hiện thường xuyên:
- Na⁺
- K⁺
- Ca²⁺
- Mg²⁺
- Al³⁺
- Zn²⁺
- Fe²⁺, Fe³⁺
Ghi nhớ nhóm này giúp xử lý nhanh phần lớn bài tập cơ bản.
Ion phi kim phổ biến
Các ion phi kim thường gặp gồm:
- Cl⁻
- F⁻
- Br⁻
- O²⁻
- S²⁻
- N³⁻
- P³⁻
Đây là các ion “trọng tâm” trong chương trình học.
Cách sử dụng bảng trong làm bài
Để tận dụng bảng hiệu quả:
- Kết hợp với quy tắc nhóm nguyên tố
- Dùng để kiểm tra nhanh kết quả
- Áp dụng khi làm bài trắc nghiệm tốc độ cao
Lưu ý: → Không nên phụ thuộc hoàn toàn vào bảng, mà cần hiểu cách suy luận
Để làm chủ cách xác định điện tích ion, bạn cần hiểu bản chất mất – nhận electron, kết hợp quy tắc nhóm nguyên tố và luyện tập qua nhiều dạng bài. Khi đã quen, việc xác định điện tích sẽ trở nên nhanh và gần như phản xạ tự nhiên.
Ion đa nguyên tử có điện tích cố định, cần ghi nhớ hoặc tra bảng như SO₄²⁻, NO₃⁻, NH₄⁺ để áp dụng nhanh.
Không cần học hết, chỉ nên nhớ ion phổ biến và dùng quy tắc electron để suy luận khi gặp nguyên tố lạ.
Dựa vào loại nguyên tố: kim loại tạo ion dương, phi kim tạo ion âm trong đa số trường hợp.
Có, đặc biệt với kim loại chuyển tiếp như Fe, Cu, điện tích phụ thuộc vào từng hợp chất cụ thể.
Ưu tiên dùng quy tắc nhóm nguyên tố, sau đó kiểm tra tổng điện tích để đảm bảo hợp chất trung hòa.